Bài giảng Hóa học 11 - Bài 3: Sự điện ly của nước pH Chất chỉ thị axit – bazơ
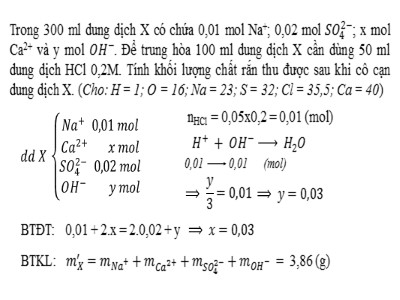
Tích số ion của nước:
Ở nhiệt độ 25oC, trong nước và các dung dịch loãng thì tích số nồng độ ion H+ và OH- là một hằng số, gọi là tích số ion của nước:
KH2O phụ thuộc vào nhiệt độ (mỗi nhiệt độ sẽ có KH2O khác nhau)
Bạn đang xem 20 trang mẫu của tài liệu "Bài giảng Hóa học 11 - Bài 3: Sự điện ly của nước pH Chất chỉ thị axit – bazơ", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
Trong 300 ml dung dịch X có chứa 0,01 mol Na+; 0,02 mol ; x mol Ca2+ và y mol . Để trung hòa 100 ml dung dịch X cần dùng 50 ml dung dịch HCl 0,2M. Tính khối lượng chất rắn thu được sau khi cô cạn dung dịch X. (Cho: H = 1; O = 16; Na = 23; S = 32; Cl = 35,5; Ca = 40)nHCl = 0,05x0,2 = 0,01 (mol)0,010,01(mol)BTĐT:0,01 + 2.x = 2.0,02 + yBTKL: = 3,86 (g)BÀI 3Sự điện ly của nướcpHChất chỉ thị axit – bazơ NỘI DUNGISỰ ĐIỆN LY CỦA NƯỚCIIpH DUNG DỊCHIIICHẤT CHỈ THỊ AXIT – BAZƠISỰ ĐIỆN LY CỦA NƯỚCH2OH++ OH-– Nước là chất điện ly rất yếu:----> Nước nguyên chất: 555 triệu phân tử nước chỉ có 1 phân tử phân ly ra ion.ISỰ ĐIỆN LY CỦA NƯỚC Tích số ion của nước:1Ở nhiệt độ 25oC, trong nước và các dung dịch loãng thì tích số nồng độ ion H+ và OH- là một hằng số, gọi là tích số ion của nước: KH2O phụ thuộc vào nhiệt độ (mỗi nhiệt độ sẽ có KH2O khác nhau) Tính axit, bazơ của một môi trường:2ISỰ ĐIỆN LY CỦA NƯỚC– Môi trường trung tính:[H+] = [OH-] = 10-7 (M)– Môi trường axit:[H+] > 10-7 (M)– Môi trường bazơ:[H+] 7[H+] = 10-7 (M)[H+] > 10-7 (M)IIpH DUNG DỊCH Công thức tính pH dung dịch:3– Dung dịch axit: – Dung dịch bazơ: Nồng độpHMôi trường[H+] = 0,1 M [H+] = 10-7 (M) [H+] = 0,025 (M)[H+] = 10-11,5 (M)= 10-1 (M)pH = 1pH = 7pH = 1,6pH = 11,5AxitAxitBazơTrung tính Khái niệm:1– Chất chỉ thị axit – bazơ là chất có màu biến đổi, phụ thuộc vào giá trị pH của dung dịch. CHẤT CHỈ THỊ AXIT-BAZƠIIIQuỳ tímPhenolphtaleinNaOHNaOHNaOHCHẤT CHỈ THỊ AXIT-BAZƠIII Một số chất chỉ thị quan trọng:2a) Quỳ tím: – Hóa đỏ: pH ≤ 6– Hóa xanh: pH ≥ 8b) dd phenolphtalein – Không màu: pH 7 là A. 1. B. 3. C. 2. D. 4.CỦNG CỐIVTHANK YOUFOR LISTENING
Tài liệu đính kèm:
 bai_giang_hoa_hoc_11_bai_3_su_dien_ly_cua_nuoc_ph_chat_chi_t.pptx
bai_giang_hoa_hoc_11_bai_3_su_dien_ly_cua_nuoc_ph_chat_chi_t.pptx



